手性是生命的核心所在,而控制一对镜像分子(对映体)中某一种的形成,是合成化学的一个基本原则。
尽管控制手性碳、硅、磷和硫立体中心是常见的,但胺中的氮立体中心通常构型不稳定。在氮手性(N-手性)选择性构建方面取得的有限成果主要集中在季铵盐和桥联双环胺上,这些化合物具有受限的锥形构型。非桥联的N-手性化合物的不对称合成,存在手性源过量的问题,并且立体选择性较差。
2025年11月12日,南方科技大学谭斌团队与加州大学洛杉矶分校K.N.Houk团队合作(吴三、陈鹏全、段梦为共同第一作者),在国际顶尖学术期刊Nature上发表了题为:Controllingpyramidalnitrogenchiralitybyasymmetricorganocatalysis的研究论文。

该研究实现了N-手性化合物的首例催化不对称合成,为后续相关研究提供了重要基础与方向
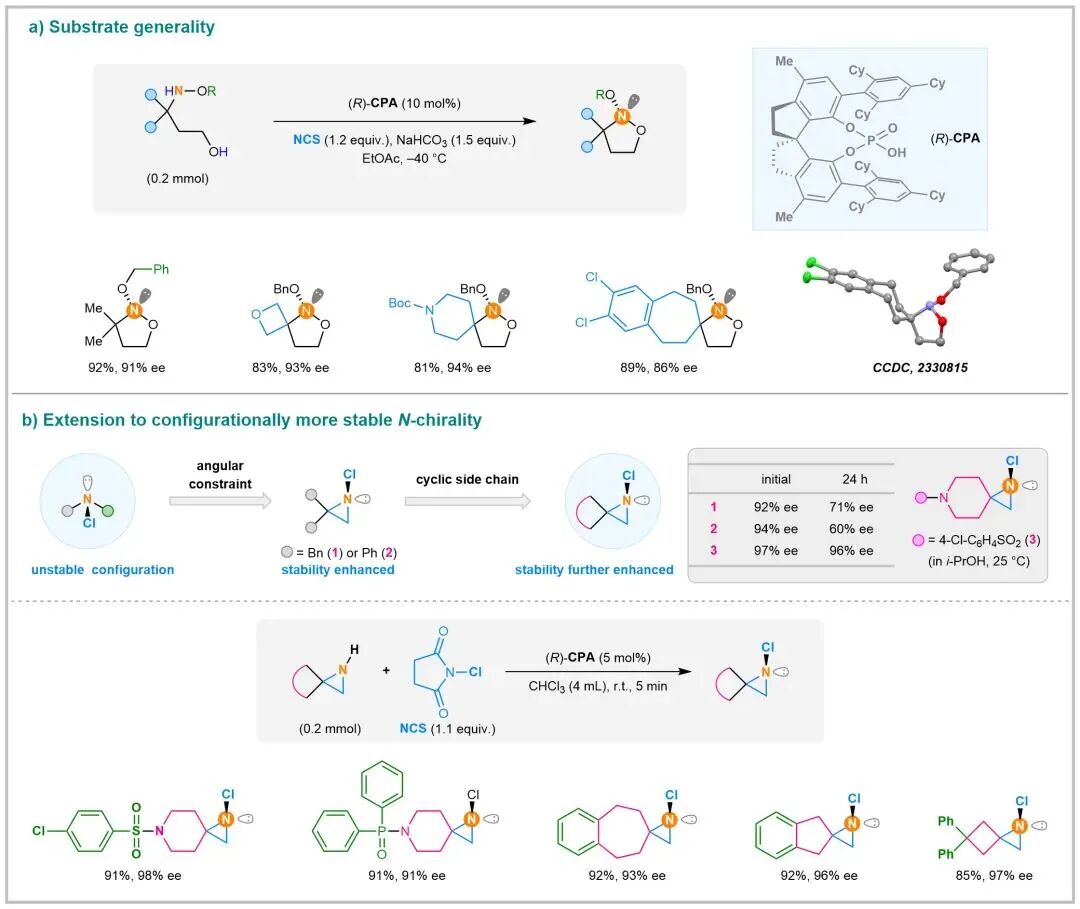
在这项新研究中,研究团队提出通过不对称氯化反应合成极具挑战性的非环状N-手性氯代羟胺。为进一步稳定并分离手性产物,研究团队设计利用亲核取代反应捕获不稳定的手性中间体B,从而获得结构和构型更稳定的N-手性分子。该过程中成功实现手性转移的关键在于亲核取代需严格遵循SN2反应机理,且反应速率应远大于中间体B的消旋速率。
然而,该设想在实施中面临三重挑战:1)氮手性中心由于孤对电子的存在及较低的空间位阻,在体系中难以实现高效、高选择性的立体化学控制;2)中间体B本身结构不稳定,易发生多种副反应;3)其较低的消旋能垒极大增加了手性转移的可操作性。
经大量尝试,研究团队基于自主开发的手性磷酸催化剂库,成功实现了羟胺类底物的催化不对称氯化反应。通过在底物中预先引入羟基,实现了反应速率显著提升的分子内亲核取代,从而顺利完成手性传递,最终获得构型稳定的N-手性化合物。
经过系统的反应条件优化,研究团队最终采用空间位阻较大的手性磷酸(CPA)作为催化剂。通过不对称卤化—分子内亲核取代两步串联反应,成功实现了21个N-立体中心为唯一手性元素的1,2-oxazolidines类化合物的高对映选择性合成,该策略展现出良好的底物适用性和官能团兼容性。所得产物的分子结构及绝对立体构型通过单晶X射线衍射分析得以确认,晶体结构清晰显示了产物中氮原子呈三角锥几何构型,并作为分子中唯一的手性元素存在。
有机催化不对称控制N-手性
尽管三元环的张力效应使N-氯代氮杂环丙烷的构型稳定性相较于无环类似物有所提高,但对于邻位含有双苄基或双苯基取代的衍生物,在室温下仍可观察到显著的消旋现象(在异丙醇中放置24小时后,对映体过量值分别下降21%和34%)。为克服这一问题,研究团队通过在氮原子邻位引入刚性螺环结构,成功实现构型稳定性的显著提升(相同条件下对映体过量值值仅损失1%)。在前期工作基础上,研究团队对反应体系进行微调,在相同手性磷酸催化下,于氯仿溶剂中反应5分钟,顺利实现了氮杂环丙烷类化合物的高对映选择性氯化反应,所得产物的对映体过量值均大于90%。
研究团队结合控制实验与DFT理论计算,对反应机理进行了深入探究,证实立体选择性决定步骤为氯化反应,后续分子内亲核取代遵循SN2机制,从而确保了手性信息的有效传递。












 川公网安备 51190202000048号
投稿交流:
川公网安备 51190202000048号
投稿交流: